Qu’est-ce que la randomisation mendélienne ?
ON PEUT RÉSUMER L’OBJET DE LA RECHERCHE MÉDICALE COMME L’ÉTUDE DE LA RELATION POTENTIELLE ENTRE UNE EXPOSITION ET UNE MALADIE. CETTE RELATION PEUT ÊTRE ÉTUDIÉE DE MANIÈRE CONTRÔLÉE, COMME DANS UN ESSAI THÉRAPEUTIQUE OU DE MANIÈRE EMPIRIQUE ET OBSERVATIONNELLE COMME DANS UNE ÉTUDE ÉPIDÉMIOLOGIQUE.
L’essai thérapeutique contrôlé randomisé en double aveugle (ETC) représente actuellement le type d’étude ayant le plus haut niveau de preuve parmi les plans expérimentaux connus, à l’exception des méta-analyses. La caractéristique essentielle de l’essai thérapeutique est que l’attribution de l’exposition à un traitement est le résultat d’un mécanisme aléatoire qui rend le traitement indépendant de toutes les caractéristiques du sujet et de son environnement. S’il y a un effet du traitement sur la maladie, on peut interpréter cet effet comme causal : le traitement étudié est à l’origine de la modification de la maladie chez ces patients.
Il y a cependant un certain nombre de situations dans la recherche sur l’humain dans lesquelles il n’est pas possible d’attribuer aléatoirement l’exposition des sujets à certains facteurs. Il en va ainsi de l’étude du rôle d’un toxique, que le sujet y soit exposé volontairement comme le tabac ou l’alcool, ou involontairement comme un élément de l’environnement tel que le radon ou les conditions de travail. Une des limites importantes de ces études observationnelles est la présence quasiment inévitable de facteurs de confusion venant perturber l’estimation de la relation entre l’exposition et la maladie. Par définition, on dit d’un facteur qu’il est facteur de confusion s’il est relié statistiquement à l’exposition étudiée et à la maladie.
Ainsi dans l’étude de l’effet du tabac sur le cancer de l’œsophage, l’alcool est un facteur de confusion car il est statistiquement relié au tabac (les buveurs fument plus que les non-buveurs, en moyenne) et à la maladie (les buveurs ont plus fréquemment un cancer de l’œsophage que les non-buveurs). Ce phénomène empêche d’affirmer que le tabac est la cause du cancer.
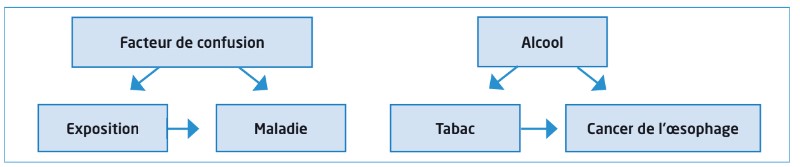
Il existe différentes méthodes pour limiter le rôle de potentiels facteurs de confusion. Ces méthodes peuvent être a priori comme la stratification ou l’appariement, ou a posteriori comme l’ajustement au cours des analyses statistiques. Le grand enjeu de toutes ces méthodes est en fait de réussir à contourner l’écueil principal des méthodes observationnelles qui est qu’en présence d’un facteur de confusion, on ne peut pas interpréter de manière causale les corrélations éventuellement constatées entre l’exposition et la maladie.
L’intérêt essentiel de l’ETC est de recourir à la randomisation laquelle permet de supprimer l’effet de confusion de certains facteurs, effet pouvant expliquer au moins partiellement l’effet constaté entre une exposition et une maladie. L’effet du tabac sur la survenue d’un AVC sera indépendant de l’effet éventuel d’un hypocholestérolémiant car la proportion de fumeurs sera la même dans les deux groupes de traitements comparés. Le tabac ne sera donc plus un facteur de confusion même si l’effet du tabac sur l’AVC sera lui toujours présent.
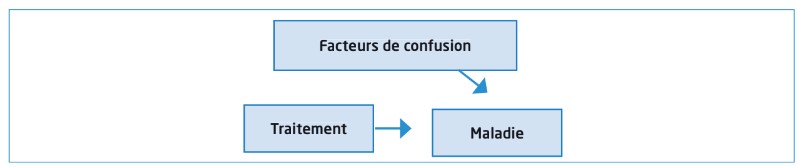
Parmi les méthodes a priori, on trouve également depuis une vingtaine d’années la randomisation mendélienne (RM). Elle est utilisée pour améliorer l’estimation et l’interprétation des effets d’une exposition d’intérêt sur l’expression de la maladie en tirant profit d’une expérience naturelle de randomisation, à savoir l’attribution aléatoire des gènes parentaux à chaque descendant. Cela permet dans une large mesure de réduire les effets de confusion. Le principe de la RM consiste à analyser l’effet d’un variant génétique en lieu et place de celui d’un facteur de risque modifiable (comme la consommation d’alcool, ou le poids) auquel il est associé. Ce variant génétique sera alors a priori indépendant de tout facteur de confusion puisqu’il leur préexiste. En supprimant cet effet de confusion, une étude par RM permet d’évaluer dans quelle mesure la relation entre l’exposition à un facteur modifiable et une maladie est causale [Sanderson].
En faisant un raccourci, la RM revient à simuler l’attribution aléatoire d’une exposition comme on pourrait la faire dans un ETC en choisissant des sujets en fonction de leurs caractéristiques génétiques. Ces gènes étant présents ou absents dès la conception, ils ne sont pas susceptibles d’être influencés ni par le facteur modifiable ni par la maladie étudiée mais ils peuvent influer sur l’expression de celle-ci.
Un premier exemple désormais classique permet d’illustrer l’idée [Davies]. Pour étudier la relation entre la consommation d’alcool et la tension artérielle (TA), on peut réaliser une RM en sélectionnant des sujets ayant sur le gène de l’aldéhyde-déshydrogénase ALDH2 l’allèle variant rs671 qui ralentit le métabolisme de l’alcool et qui est à l’origine des manifestations d’intolérance à l’alcool (flush). On compare ces sujets à ceux ayant la forme sauvage du gène permettant une métabolisation normale de l’alcool. Du fait de leur intolérance, les sujets homozygotes pour le variant ne consomment quasiment pas d’alcool. Si l’on montre par ailleurs que ces sujets ont moins souvent de l’hypertension artérielle, on peut en déduire un rôle très probablement causal de la consommation d’alcool sur la tension artérielle [Chen]. Une étude observationnelle classique aurait du mal à isoler l’effet propre de la consommation d’alcool sur la tension artérielle dans la mesure où la tension artérielle pourrait être modifiée par des facteurs de confusion comme le tabac qui sont également associés à la consommation d’alcool.
La causalité ne peut cependant pas être affirmée, du moins pas sans faire quelques hypothèses complémentaires. Il faut d’abord que le variant génétique soit associé au facteur de risque étudié. C’est évident dans le cas de l’alcool déshydrogénase et de l’alcool, mais ça l’est moins dans d’autres cas comme nous le verrons plus loin. Il faut ensuite qu’il n’y ait effectivement pas de facteur de confusion résiduel qui puisse expliquer le lien entre le variant génétique et la maladie. Par exemple, d’autres gènes, hérités simultanément au variant rs671 de l’ALDH2 pourraient expliquer un effet sur la tension artérielle. Enfin, il faut admettre que le variant n’agit sur la maladie que par l’intermédiaire du facteur de risque et par aucun autre intermédiaire. Le variant ne doit pas modifier la consommation d’autres facteurs pouvant modifier la tension artérielle.
Les cas où un variant unique peut expliquer la totalité de l’effet sont en fait assez rares et la plupart du temps il faudra passer par la combinaison des effets de plusieurs variants pour évaluer l’effet de l’exposition sur la maladie. On utilise alors les grandes bases de données génétiques modernes décrivant le génome entier de milliers de sujets. Ces bases fournissent entre autres les polymorphismes ou variants d’un seul nucléotide (PSN ou SNP en anglais, pour Single Nucleotide Polymorphism), lesquels polymorphismes sont plus de 600 millions, dispersés sur tout le génome. Ils expliquent près de 90% de la variabilité phénotypique de l’humain. La plupart des chaînes métaboliques ont une efficacité modulée par ces multiples PNS et la RM peut s’appuyer sur ces variants. Il y a ainsi des types de RM dans lesquelles on utilise un ensemble de ces variants qui, collectivement, expliquent une part plus grande de la variabilité et donc de l’expression de la maladie. Ces études peuvent notamment évaluer l’effet d’expositions volontaires à un toxique comme le tabac.
Ainsi, Park et al. ont étudié à l’aide d’une MR l’effet du tabac sur la survenue d’un cancer du sein. Cette relation est en effet encore débattue en raison de l’effet modeste et inconstant du tabac décrit dans différentes études observationnelles classiques. En utilisant des bases génétiques, les auteurs ont identifié deba une série de plusieurs dizaines de PSN associés soit au nombre de cigarettes consommées par jour soit à l’index de tabagisme vie entière, intégrant la durée et la quantité de cigarettes consommées sur une vie. Ils montrent ainsi un lien statistique entre le tabagisme mesuré de deux manières différentes et la survenue d’un cancer du sein, avec une interprétation là aussi quasiment causale de cette relation car débarrassée de l’effet de confusion de tiers-facteurs.
LIMITES DES ÉTUDES DE RM
Les études basées sur la RM présentent un certain nombre de limites. Tout d’abord, elles ne portent que sur des facteurs de risque modifiables. On ne peut donc pas les utiliser pour évaluer l’effet d’un facteur purement environnemental comme l’effet du radon ou des conditions climatiques.
Les effets mis en évidence sont souvent d’ampleur très limitée, n’expliquant souvent que 1 à 2 % de la variabilité phénotypique d’une maladie. Ainsi dans l’étude de Guo sur le lien entre l’indice de masse corporelle (IMC) et la survie du cancer du sein, le score génétique basé sur les PNS sélectionnés n’explique que 1,6% de la variabilité de l’indice de masse corporelle et ce score est lui-même associé à un hasard ratio de 1,11 pour la survie au cancer du sein, ce qui est assez faible par rapport à l’effet de la plupart des traitements actuels ou d’autres facteurs de risque, malgré l’interprétation causale entre l’IMC et la survie possible grâce à la RM.
CONCLUSION
Les études avec RM sont donc un intermédiaire entre l’essai randomisé et l’étude observationnelle. Elles visent à permettre une interprétation causale de la relation constatée entre un facteur de risque modifiable et une maladie en limitant fortement les effets de potentiels facteurs de confusion. Mais dans la mesure où elles ne sont pas véritablement randomisées et qu’elles reposent sur un certain nombre d’hypothèses complémentaires, elles ne constituent donc pas une panacée, même si leur niveau de preuve peut être considéré comme étant en moyenne plus élevé que celui des études purement observationnelles.
Nicolas Meyer1,2, PU-PH.
1. GMRC, Pôle de santé publique – Santé au Travail – Hygiène Hospitalière – CIC, Hôpitaux Universitaire de Strasbourg, Strasbourg.
2. iCUBE, CNRS UMR 7357, Illkirch-Graff enstaden.
RÉFÉRENCES
– Chen L, Davey Smith G, Harbord RM, Lewis SJ. Alcohol intake and blood pressure: a systematic review implementing a Mendelian randomization approach. PLoS ed 2008;5:e52. doi:10.1371/journal.pmed.0050052
– Davies NM, Holmes MV, Smith GD. Reading Mendelian randomisation studies: a guide, glossary, and checklist for clinicians. BMJ 2018;362:k601 http:// dx.doi.org/10.1136/bmj.k601.
– Guo Q, Burgess S, Turman C et al. Body mass index and breast cancer survival: a Mendelian randomization analysis. International Journal of Epidemiology, 2017, 1814–1822 doi: 10.1093/ije/dyx131. – anderson E, Glymour MM, Holmes MV et al. Mendelian randomization. Nat Rev Methods Primers. 2022 Feb 10:2:6.doi: 10.1038/s43586-021-00092-5.






2 commentaires