Hyperémèse gravidique
LES NAUSÉES ET VOMISSEMENTS DE LA GROSSESSE REPRÉSENTENT L’UN DES SYMPTOMES LES PLUS FRÉQUENTS DU 1ER TRIMESTRE DE LA GROSSESSE. LORSQUE CES NAUSÉES ET VOMISSEMENTS DEVIENNENT INVALIDANTS, ALTÈRENT LA VIE QUOTIDIENNE OU L’ACTIVITÉ PROFESSIONNELLE ET AFFECTENT NÉGATIVEMENT LES RELATIONS FAMILIALES, IL S’AGIT ALORS D’UNE HYPERÉMÈSE GRAVIDIQUE (HG). CET ARTICLE S’APPUIE SUR LES CONCLUSIONS DE LA CONFÉRENCE FORMALISÉE D’EXPERT DU COLLÈGE NATIONAL DES GYNÉCOLOGUES ET OBSTÉTRICIENS FRANÇAIS ÉLABORÉES EN 2020 ET PUBLIÉES EN 20211 ET LA COMPLÈTE DES DONNÉES RÉCEMMENT PARUES.
DÉFINITION
L’évaluation des symptômes des nausées et vomissements au 1er trimestre s’appuie sur la perte de poids, les signes de déshydratation et le score PUQE modifié (Pregnancy Unique Quantification of Emesis and nausea) (Encadré 1). Les nausées et vomissements gravidiques sont considérés comme non compliqués lorsque la perte de poids est < 5%, sans signes cliniques de déshydratation et un score PUQE est ≤ 6. L’HG, incluant les formes modérées à sévères, est défi nie par la conférence formalisée d’experts (CFE) comme des nausées et vomissements gravidiques associés à au moins un des signes de l’encadré 2. Cette définition rejoint la majorité de celles Encadré 1. Score PUQE modifié des sociétés savantes internationales2–4 mais n’aborde pas complétement la maladie dans son intégralité. C’est pourquoi, f i n 2021, un groupe incluant des chercheurs, des femmes ayant vécu une HG et leurs familles, des professionnels de la périnatalité (obstétriciens, gynécologues, sage-femmes) et d’autres professionnels de la santé impliqués dans la prise en charge des femmes atteintes d’HG (médecins généralistes, diététiciens, infirmières) ont proposé une définition qui va au-delà des seuls symptômes digestifs, incluant : l’apparition des symptômes en début de grossesse (avant 16 semaines d’aménorhée), des nausées ou vomissements sévères ; une incapacité à manger ou à boire normalement ; une limitation importante des activités de la vie quotidienne ou des signes de déshydratation5.

ÉPIDÉMIOLOGIE
La fréquence de L’HG est mal connue et se heurte à l’absence d’études solides. 30 à 35 % des femmes auraient une altération de leur bien être en raison des symptômes. Les vomissements incoercibles concerneraient 0,3 à 3,6% des grossesses.
FACTEURS DE RISQUE ET MÉCANISMES
Les mécanismes expliquant l’HG sont mal compris. Les causes sont probablement multifactorielles et peuvent varier d’une femme à l’autre. En premier lieu, il convient d’écarter l’hypothèse d’une étiologie psychologique à l’HG et d’abandonner l’idée que ces femmes rejettent leur grossesse ou somatisent des troubles psychiques.
De nombreux facteurs de risque ont été proposés : portage d’Helicobacter Pylori, prédisposition génétique, faible indice de masse corporelle, fœtus de sexe féminin, grossesses multiples1,6 mais leur rôle reste incertain.
La théorie hormonale est probablement la plus solide. De travaux se sont intéressés à l’hormone chorionique gonadotrophique humaine (hCG), aux hormones thyroïdiennes et stéroïdiennes comme le cortisol, les œstrogènes et la progestérone au début de la grossesse, car l’apparition et le pic des symptômes sont en corrélation avec les élévations de plusieurs de ces hormones1,6. La voie la plus pertinente semble être celle du Growth Differenciation Factor 15 (GDF15) (Figure 1) qui est un marqueur de la cachexie et affecte l’appétit et la perception du goût.
Les femmes souffrant d’HG présentent des variants dans les gènes codant pour la protéine placentaire GDF15 et ses récepteurs hormonaux (GFRAL)7,8. Petry C.J. et al ont démontré que les concentrations circulantes de GDF15 étaient plus élevées chez les femmes signalant des vomissements que chez les femmes ne signalant aucune nausée ou vomissement pendant la grossesse. Ils ont également constaté que les concentrations sériques de GFD15 étaient fortement corrélées positivement avec les niveaux d’hCG suggérant un lien entre ces deux hormones9.
CONSÉQUENCES DE L’HYPÉRÈMESE GRAVIDIQUE
La survenue d’une HG est associée à un risque accru de petit poids de naissance, de petit poids pour l’âge gestationnel et de naissance prématurée1. Cependant, la qualité des études et l’absence de prise en compte d’éventuels biais ne permettent pas de conclure à une véritable association et encore moins à un possible lien de causalité. Chez la mère, il existe un risque d’encéphalopathie de Gayet-Wernicke, en particulier en cas de réhydratation sans ajout de vitamine B1 dont les conséquences peuvent être irréversibles1. Rarement, la carence en vitamine K peut entraîner un syndrome de Binder1.
L’HG peut avoir des conséquences psychologiques et psychiatriques (stress, troubles anxio-dépressifs, état de stress post-traumatique et idées suicidaires) durant la grossesse et le post-partum1. La sévérité des symptômes peut parfois amener certaines femmes à envisager une interruption volontaire de grossesse non souhaitée initialement ou les amener à renoncer à une grossesse ultérieure1.
Enfin, il existe un risque de récidive lors d’une grossesse ultérieure avec fréquence comprise entre 15 et 81 %10.
BILAN
En cas d’HG, il faut effectuer un ionogramme, une créatininémie et une bandelette urinaire complète afin de rechercher des éléments de sévérité1. En cas de persistance et/ou d’aggravation des symptômes après un traitement bien conduit, il convient d’éliminer un diagnostic différentiel au travers de l’interrogatoire, de l’examen clinique et la réalisation d’un dosage des transaminases, de la lipase, de la CRP, de la TSH, de la T4, d’une numération leucocytaire et d’une échographie abdominale.
PRISE EN CHARGE
L’HG est une pathologie complexe et difficile à traiter
• Prise en charge non médicamenteuse
Les techniques de prise en charge non médicamenteuse (gingembre, vitamine B6, acupuncture, acupression) sont à réserver aux femmes avec des formes non compliquées. L’aromathérapie n’est pas à utiliser. Globalement, ces méthodes n’ont pas leur place dans la prise en charge de l’HG.
• Règles hygiéno-diététiques
Les femmes peuvent adapter librement leur régime alimentaire et leur mode de vie en fonction de leurs symptômes. Aucune modification du régime alimentaire ou du mode de vie n’a prouvé son efficacité pour améliorer les nausées et vomissements gravidiques et l’HG.1
Les modifications des habitudes de travail, l’activité physique, le repos en journée et le coucher plus tôt pourraient améliorer les nausées et vomissements gravidiques mais les données concernant l’efficacité de ces interventions sont faibles en qualité1. Il est conseillé aux femmes présentant des nausées et vomissements gravidiques d’arrêter leurs vitamines prénatales et leur supplémentation en fer et de privilégier la supplémentation en acide folique seule car la supplémentation en fer au 1er trimestre de la grossesse semble aggraver les symptômes1.
• Prise en charge médicamenteuse
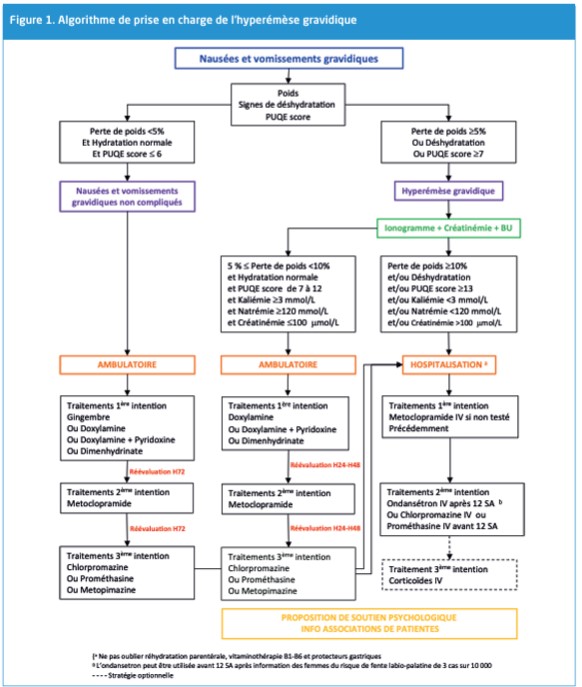
En cas d’HG, il convient de proposer une prise en charge médicamenteuse en testant les molécules seules ou en association : doxylamine, doxylamine-pyridoxine, métoclopramide, dimenhydrinate, phénothiazines (chlopromazine et prométhazine), ondansetron, corticoïdes. Aucune n’a réellement démontré de supériorité par rapport à une autre à réduire les symptômes des nausées et vomissements et de l’HG. Par ailleurs, seule l’association Doxylamine-Pyridoxine a fait l’objet d’études versus placebo11–14. Sur la base de ces éléments et de leurs limites, le groupe de travail de la CFE a proposé que soient toujours choisis pour des utilisations en première, deuxième, ou troisième intention, les médicaments ou les associations de médicaments associés aux effets secondaires les moins sévères et les moins fréquents. Il a également proposé un algorithme de prise en charge selon la sévérité des symptômes (Figure). La place de l’ondansetron est particulière puisque cette molécule a fait l’objet d’une alerte de l’agence nationale de sécurité du médicament (ANSM) en raison d’une augmentation minime mais significative du risque absolu de fentes labio-palatines lors de l’exposition à l’ondansétron en période d’organogénèse de l’ordre de 3 cas supplémentaires pour 10 000 naissances vivantes exposées. En reprenant l’ensemble des données disponibles, Coulm B. indiquent que les préconisations qui conduisent à écarter formellement l’ondansetron de la stratégie thérapeutique des vomissements gravidiques sévères au 1er trimestre de la grossesse ne paraissent pas opportunes15. Ainsi, bien que l’ondansétron n’ait pas l’AMM pour la prise en charge des vomissements gravidiques, son utilisation est possible au premier trimestre mais doit rester limitée aux situations pour lesquelles les autres thérapeutiques ont été un échec. Il est utilisable sans restriction au 2ème et au 3ème trimestre.
• Traitements complémentaires
Les traitements antiémétiques peuvent être complétés d’une prescription d’inhibiteurs de la pompe à protons à visée gastrique. Une hydratation parentérale est indispensable dans les formes sévères. Elle fait appel au sérum salé isotonique plus qu’au sérum glucosé16. De la vitamine B1 doit être systématiquement administrée.
• Hospitalisation
Une hospitalisation peut être proposée en cas d’HG lorsqu’elle est associée à au moins un des critères de l’encadré 3.
Cependant, ces critères ne doivent pas être interprétés de façon stricte. L’association de plusieurs anomalies biologiques ne franchissant pas les seuils présentés peut aussi conduire à une hospitalisation.

Une altération globale physique ou psychologique de la patiente ou une intolérance alimentaire totale peuvent aussi conduire à envisager l’hospitalisation.
Une prise en charge similaire peut être effectuée à domicile en s’appuyant sur des prestataires et des infirmiers libéraux mais le suivi des symptômes et de l’évolution peut être plus difficile.
Après l’hospitalisation, il est important d’organiser une prise en charge ambulatoire qui s’articulera autour d’un médecin réfèrent afin de tenter de réduire le risque de récidive sévère et de ré-hospitalisation.
Accompagnement des femmes atteintes d’hyperémèse gravidique
Il ne faut plus les mettre à l’isolement (mise dans le noir, confiscation du téléphone portable ou interdiction de visites…) en raison de l’absence de données suggérant une quelconque efficacité de cette mesure et de possibles effets psychologiques délétères.
Les conséquences psychologiques et psychiatriques de l’HG peuvent être sévères, le soutien psychologique doit être encouragé. De plus, il convient d’informer les femmes souffrant d’HG de l’existence d’associations de patientes investies dans l’accompagnement de ces femmes et de leur entourage.
En France, deux associations sont engagées sur cette thématique : association de lutte contre l’hyperémèse gravidique https:// www.associationhg.fr et 9 mois avec ma bassine https://www.facebook.com/9moisavecmabassine/?locale=fr_FR.
Philippe Deruelle, Loïc Sentilhes, Louise Ghesquière, Raoul Desbrière, Guillaume Ducarme, Luisa Attali, Annic Jarnoux, France Artzner, Audrey Tranchant, Thomas Schmitz, Marie-Victoire Sénat, Montpellier
philippe.deruelle@chu-montpellier.fr
RÉFÉRENCES
1. [Expert consensus from the College of French Gynecologists and Obstetricians: Management of nausea and vomiting of pregnancy and hyperemesis gravidarum] – PubMed [Internet]. [cité 2 juill 2023]. Disponible sur: https://pubmed.ncbi.nlm.nih.gov/36150647/
2. Erick M, Cox JT, Mogensen KM. ACOG Practice Bulletin 189: Nausea and Vomiting of Pregnancy. Obstet Gynecol. mai 2018;131(5):935.
3. RCOG [Internet]. [cité 24 juin 2022]. The Management of Nausea and Vomiting of Pregnancy and Hyperemesis Gravidarum (Green-top Guideline No.69). Disponible sur: https://www.rcog.org.uk/guidance/browse-all-guidance/green-top-guidelines/the-management-of-nausea-and-vomiting-of-pregnancy- and-hyperemesis-gravidarum-green-top-guideline-no-69/
4. Campbell K, Rowe H, Azzam H, Lane CA. The Management of Nausea and Vomiting of Pregnancy. J Obstet Gynaecol Can JOGC J Obstet Gynecol Can JOGC. déc 2016;38(12):1127-37.
5. Jansen LAW, Koot MH, van’t Hooft J, Dean CR, Bossuyt PMM, Ganzevoort W, et al. The windsor definition for hyperemesis gravidarum: A multistakeholder international consensus definition. Eur J Obstet Gynecol Reprod Biol. 1 nov 2021;266:15-22.
6. Deruelle P, Dufour P, Subtil D, Houfflin-Debarge V, Dherbomez A, Wemeau JL, et al. [Hyperemesis in the first trimester of pregnancy: role of biological hyperthyroidism and fetal sex]. Gynecol Obstet Fertil. mars 2002;30(3):204-9.
7. Fejzo MS, Sazonova OV, Sathirapongsasuti JF, Hallgrímsdóttir IB, Vacic V, MacGibbon KW, et al. Placenta and appetite genes GDF15 and IGFBP7 are associated with hyperemesis gravidarum. Nat Commun. 21 mars 2018;9(1):1178.
8. Fejzo MS, MacGibbon KW, First O, Quan C, Mullin PM. Whole-exome sequencing uncovers new variants in GDF15 associated with hyperemesis gravidarum. BJOG Int J Obstet Gynaecol. oct 2022;129(11):1845-52.
9. Petry CJ, Ong KK, Burling KA, Barker P, Goodburn SF, Perry JRB, et al. Associations of vomiting and antiemetic use in pregnancy with levels of circulating GDF15 early in the second trimester: A nested case-control study. Wellcome Open Res. 21 sept 2018;3:123.
10. Dean CR, Bruin CM, O’Hara ME, Roseboom TJ, Leeflang MM, Spijker R, et al. The chance of recurrence of hyperemesis gravidarum: A systematic review. Eur J Obstet Gynecol Reprod Biol X. janv 2020;5:100105.
11. Koren G, Clark S, Hankins GDV, Caritis SN, Miodovnik M, Umans JG, et al. Effectiveness of delayed-release doxylamine and pyridoxine for nausea and vomiting of pregnancy: a randomized placebo controlled trial. Am J Obstet Gynecol. déc 2010;203(6):571.e1-7.
12. Koren G, Hankins GDV, Clark S, Caritis SN, Miodovnik M, Umans JG, et al. Effectiveness of doxylamine-pyridoxine for morning sickness. Am J Obstet Gynecol. mai 2016;214(5):664-6.
13. Koren G, Clark S, Hankins GDV, Caritis SN, Umans JG, Miodovnik M, et al. Demonstration of early efficacy results of the delayed-release combination of doxylamine-pyridoxine for the treatment of nausea and vomiting of pregnancy. BMC Pregnancy Childbirth. 24 nov 2016;16(1):371.
14. Persaud N, Meaney C, El-Emam K, Moineddin R, Thorpe K. Doxylamine-pyridoxine for nausea and vomiting of pregnancy randomized placebo controlled trial: Prespecified analyses and reanalysis. PloS One. 2018;13(1):e0189978.
15 Coulm B. [Nausea and vomiting in pregnancy: A place for ondansetron?]. Gynecol Obstet Fertil Senol. déc 2021;49(12):947-50.
16. [Deruelle P, Sentilhes L, Schmitz T, Sénat MV in reply to the correspondence by J. Boujenah on the article entitled « Consensus Formalisé d’Experts du
Collège National des Gynécologues et Obstétriciens Français: Prise en charge des nausées et vomissements gravidiques et de l’hyperémèse gravidique »
Gynecol Obstet Fertil 2022; 50(11): Doi:10.1016/j.gofs.2022.09.002] – PubMed [Internet]. [cité 2 juill 2023]. Disponible sur: https://pubmed.ncbi.nlm.nih. gov/36195288/
17. Deruelle P, Sentilhes L, Ghesquière L, Desbrière R, Ducarme G, Attali L, et al. [Expert consensus from the College of French Gynecologists and Obstetricians: Management of nausea and vomiting of pregnancy and hyperemesis gravidarum]. Gynecol Obstet Fertil Senol. nov 2022;50(11):700-11.