Les saignements utérins anormaux représentent un symptôme extrêmement fréquent en gynécologie. Ses causes sont multiples et variées, organiques ou fonctionnelles. La frontière entre les deux est parfois difficile à cerner. Nous abordons ici les ménorragies fonctionnelles et leurs principales options thérapeutiques médicales.
Les ménorragies représentent 30% environ des motifs de consultation en gynécologie. Elles ont des conséquences multiples négatives sur la qualité de vie des femmes concernées. Tant par l’inconfort créé par ces pertes de sang, parfois cataclysmiques que par les anémies ferriprives chroniques souvent méconnues
Quelques définitions1, 2
Les ménorragies font partie des saignements utérins anormaux. Ces saignements ne résument pas, loin s’en faut, les troubles du cycle chez la femme. Rappelons ici la signification des différents mots habituellement utilisés pour les caractériser :
– Les spanio-ménorrhées sont des saignements irréguliers survenant dans des intervalles de plus de 35 jours
– Les oligoménorrhées sont des saignements réguliers, règles de faible importance
– Les ménorragies sont des épisodes hémorragiques réguliers, règles supérieures à 80 ml et/ou dont la durée est supérieure à 5 jours
– Les métrorragies sont des saignements en dehors des règles
– Les méno-métrorragies sont des épisodes fréquents de saignements excessifs et prolongés survenant à des moments irréguliers, lors des règles et en dehors des règles
– Les polyménorrhées sont des épisodes réguliers et fréquents survenant à des intervalles de moins de 21 jours)
– Les saignements utérins fonctionnels sont des saignements anormaux en l’absence de toute pathologie organique décelée ou confirmée
Les causes des saignements utérins anormaux (SUA) : organiques ou fonctionnels ?
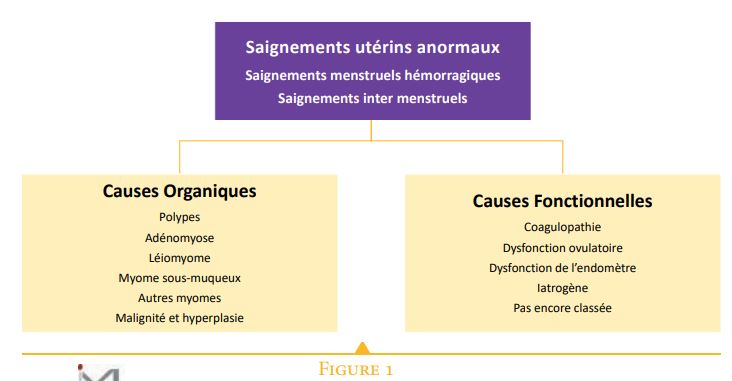
Elles sont bien résumées par la nomenclature FIGO PALM-COEIN3 (Figure 1) qui distingue les causes organiques : les polypes, l’adénomyose, les myomes intracavitaires et interstitiels, l’hyperplasie et les cancers, GEU & grossesses et les causes fonctionnelles : les infections, les coagulopathies, les syndromes ovulatoires, les causes endométriales non organiques…
Affirmer une origine organique n’est pas toujours simple, en effet un fibrome de type 3 qui affleure la cavité ou une adénomyose modérée sont-ils ou non la cause du saignement ?
Ménorragies : comment faire le diagnostic ?
1. L’interrogatoire est fondamental
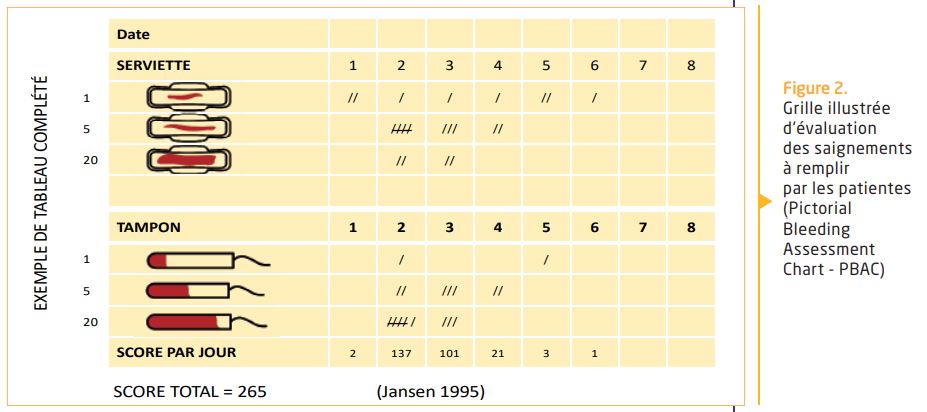
Le simple fait qu’une femme se plaigne de saignements trop abondants devrait nous su re et le score des pictogrammes (PBAC) se révèle le plus souvent inutile. Cependant nombre de femmes vivent avec des saignements qu’elles pensent être normaux : en l’absence de comparaison possible force est donc d’utiliser un score (Figure 2) et/ou de rechercher une anémie ou une carence martiale.
Un score > 100 dans les 8 premiers jours des règles représente une perte excessive de sang menstruel.
2. Lorsque ces saignements ne sont pas habituels,il faut éliminer une grossesse et une infection en première intention.
3. L’échographie endo-vaginale est l’examen clé de première intention.
Elle est susceptible d’identifier 4 types d’anomalies :
1. Les polypes
2. L’hypertrophie de l’endomètre
3. Les myomes
4. L’adénomyose
4. Biologie
La recherche d’un trouble de la coagulation sera réalisée chez l’adolescente ménorragique. Un bilan sanguin de départ comprenant une formule sanguine avec plaquettes, un bilan ferrique, un temps de prothrombine, un temps de céphaline activée aPTT, la mesure du fibrinogène ainsi qu’une évaluation de la fonction plaquettaire par un PFA (Platelet Function Analyser), équivalent du temps de saignement in vitro. En fonction de la suspicion diagnostique et des premiers résultats, des examens complémentaires pourront être effectués. 4 L’anomalie la plus fréquente est la baisse du facteur von Willebrand : elle touche environ 1% de la population. Mais d’autres anomalies peuvent être également identifiées.
5. L’IRM pelvienne
L’échographie endovaginale suffit en principe au diagnostic. Mais l’IRM garde sa place en cas de doute après suspicion de polype ou d’adénomyose ou de souhait de cartographie des myomes en prévision préopératoire de myomectomie ou encore chez les femmes vierges.
6. La biopsie de l’endomètre
Elle est surtout réalisée si l’on est dans le contexte d’hypertrophie endométriale (endomètre > 12 mm en échographie), chez les obèses, diabétiques, nullipares. Les ménorragies sont associées dans un petit pourcentage de cas (< 5%) à un risque d’hyperplasie atypique ou de cancer de l’endomètre.
7. L’hystéroscopie sera parfois nécessaire pour confirmer un diagnostic ou réaliser un geste concomitant
Quels sont les différents traitements des ménorragies ?
Une fois le diagnostic fait de la cause des ménorragies, organiques ou fonctionnelles, nous disposons de nombreuses options thérapeutiques qui dépendent de l’étiologie, de l’âge, de la parité, du souhait de la femme de conserver sa fécondité, du choix personnel de la femme de conserver ou non son utérus (à respecter absolument dans la mesure du possible).
1. Les traitements chirurgicaux et radio interventionnels
– L’endomètrectomie
– La myomectomie pour les myomes de type 0,1,2,3 ; réalisée par laparotomie, par cœlioscopie ou au mieux si faisable par voie vaginale.
– L’hystérectomie : per cœlioscopie, par voie vaginale ou par laparotomie (60 000 interventions en France par an)
– L’embolisation des myomes (EAU).
2. Nous allons développer plus avant Les traitements médicaux, uniques ou associés entre eux, en fonction de l’étiologie. L’arrêt de commercialisation de l’ulipristal acétate 5 mg (Esmya®) en raison de son hepatoxicité rare mais grave, l’alerte ANSM sur le risque d’augmentation de l’incidence des méningiomes sous macroprogestatifs ont récemment beaucoup réduit les options thérapeutiques médicales des ménorragies.
Nous disposons :
– d’antifibrinolytiques : l’acide tranexamique,
– D’un AINS : l’acide méfénamique, ayant l’indication « ménorragies fonctionnelles »
– D’analogues du LHRH avec une utilisation en principe limitée à 6 mois avec ou sans add back therapy
– De progestatifs
Les macro-progestatifs ont été très utilisés dans l’indication ménorragies en France jusqu’en 2019/2020, surtout en raison de leurs propriétés antigonadotropes qui entrainent une hypoestrogénie chronique. Dans le prolongement de l’alerte donné par Froelich en 2008,5 puis définitivement confirmé par l’étude GIS EPI- PHARE6 quant au risque augmenté de méningiomes induit par l’administration d’acétate de cyprotérone, 2 molécules supplémentaires sont aujourd’hui sur la sellette quant à ce risque : l’acétate de nomégestrol et de chormadinone.
En 2020 l’étude EPI-PHARE du GIS7 (Groupement d’Intérêt Scientifi que) constitué par l’ANSM et la CNAM), concerne l’acétate de nomégestrol et de chormadinone.
Brièvement l’étude montre que :
– Pour l’acétate de nomégestrol, le risque de méningiome est multiplié par 3,3 pour les femmes exposées à plus de 6 mois d’utilisation, en comparaison aux femmes non exposées. Une forte relation dose-effet est observée et le risque de méningiome opéré est multiplié par 12,5 après 5 ans de traitement à une posologie de 5 mg par jour, 20 jours par mois.
– Pour l’acétate de chormadinone, le risque est multiplié par 3,4 pour les femmes exposées à plus de 6 mois d’utilisation, en comparaison aux femmes non exposées. Une forte relation dose e et est observée et le risque de méningiome opéré est multiplié par 7 après 3,5 ans de traitement à une posologie de 10 mg par jour, 20 jours par mois.
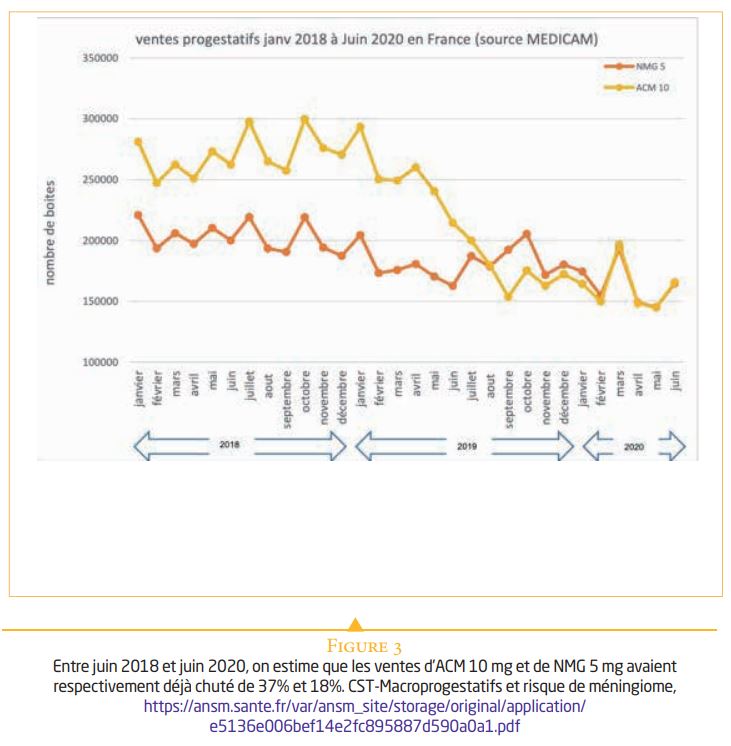
Les RCP de l’acétate de nomégestrol et de chormadinone ont été modifiés par l’ANSM et leur indication pour les « hémorragies fonctionnelles et les ménorragies liées aux myomes en pré opératoire » ne peuvent désormais être envisagées que « lorsque les alternatives thérapeutiques ont échoué ou sont contre indiquées ». Présumant des résultats de cette étude, la prescription de ces 2 progestatifs avaient d’ailleurs déjà commencé de chuter il y a 2 ans (Figure 3).
Par ailleurs l’utilisation supérieure à 4 ans a été associée dans l’étude EPIC à un risque relatif de 1,4 de cancer du sein chez les femmes en péri ménopause. Lors d’une conférence de presse le Collège National des Gynécologues Obstétriciens Français (CNGOF) a émis de nouvelles recommandations8 sur la prise en charge des saignements utérins anormaux (ménorragie) et des pathologies associées (fi bromes, endométriose…).
Le Collège constate que les options médicamenteuses sont désormais limitées et donne davantage de place aux approches chirurgicales, comme l’endomètrectomie ou l’embolisation des artères utérines. Israël Nisand a cependant précisé, lors de cette conférence de presse que le CNGOF n’approuve pas les récentes restrictions d’utilisation de ces 2 progestatifs : « C’est ignorer que l’hystérectomie est associée à des complications graves, qui ne sont pas rares » a-t-il précisé en regrettant que le CNGOF n’ait pas été consulté avant les conclusions de l’ANSM « Pour éviter un méningiome pour 10 millions de patientes, l’ANSM nous fait faire des dizaines d’hystérectomies. Nous ne sommes plus dans une évaluation de la balance bénéfices/risques ». Il a indiqué qu’un communiqué était en préparation « pour contester le fait de ne pas avoir été écouté sur ce point ».
LES DIU HORMONAUX : UNE SOLUTION BRILLANTE AUX MÉNORRAGIES FONCTIONNELLES
Ils doivent être prescrits en première intention pour l’adénomyose et les ménorragies fonctionnelles car cette stratégie a montré son efficacité et se positionne depuis de nombreuses années comme un des traitements de choix. La libération de lévonorgestrel permet une réduction du flux
sanguin de 94%. Et on a montré que ce type de traitement permet d’éviter une hystérectomie dans 80% des cas.9
L’intérêt théorique et réel, est d’apporter le progestatif localement ce qui devrait donner « le beurre et l’agent du beurre » à savoir avoir un effet progestatif à action locale efficace et permettant d’éviter une action systémique, donc sans risque d’augmentation des méningiomes, des cancers du sein et des risques coronariens. Ainsi :
– Pour le cancer du sein, une méta analyse récente ne trouve pas de lien entre le port de DIU hormonaux et la survenue de cancers du sein.10
– Pour les méningiomes, les risques avec les progestatifs incriminés sont liés à la dose cumulée reçue qui ici est infime en terme systémique. La classe du progestatif utilisé dans ce DIU n’est pas incriminée dans les études sur le méningiome.
– De plus, le DIU hormonal diminuerait les risques de cancer de l’endomètre RR=0,22(0,13-0,40) et de l’ovaire RR=0,53 (0,32-0,88).11
– Pour les risques coronariens et d’accidents vasculaires cérébraux, le DIU hormonal n’a fait l’objet d’aucune mise en garde.
En termes de tolérance, des troubles de l’humeur, une peau grasse et de l’acné ont été décrits. Ces effets secondaires surviennent chez des femmes prédisposées et sont limités le plus souvent dans le temps au premier mois de port du fait probable d’un passage systémique du lévonorgestrel plus marqué qui se régularisera rapidement ensuite.12
Les DIU hormonaux sont disponibles en 3 dosages de lévogestrel (LNG) : 13,5 mg ; 19,5 mg et 52 mg. Les trois dosages sont contraceptifs. Seul le dernier dosage est recommandé dans le traitement des ménorragies et il est commercialisé sous deux marques Miréna® et tout prochainement Donasert®. Ils peuvent être proposés en dehors d’une demande contraceptive. Leur mode d’action principal est lié à un effet local de libération du LNG.
Une étude comparative multicentrique de phase 3 randomisée de non-infériorité en simple aveugle ne trouve aucune différence d’efficacité et de tolérance entre les deux SIU LNG 52 mg, Mawet 2014 (étude HMB).
Les recommandations actuelles du CNGOF nous disent : chez une femme adulte ayant des ménorragies idiopathiques et ne souhaitant pas de grossesse à court terme, il est recommandé de proposer en première intention un traitement par DIU LNG 52mg (en l’absence de contre-indication). Enfin : le DIU LNG 52 mg est supérieur aux traitements hormonaux et non hormonaux par voie orale sur la perte sanguine, la qualité de vie et la satisfaction.13
Finalement
– Chez une femme adulte de moins de 42 ans ayant des ménorragies idiopathiques et ne souhaitant plus conserver ses possibilités de procréation en l’absence de contre-indication il est recommandé de proposer en première intention un traitement par DIU LNG 52 mg en raison de son efficacité et de son bénéfice non contraceptif.
– Le risque d’hystérectomie secondaire est plus important après chirurgie conservatrice versus DIU LNG chez les femmes jusqu’à 42 ans.13
– Chez une femme de plus de 42 ans ayant des ménorragies idiopathiques souhaitant conserver son utérus mais pas ses possibilités de procréation il est recommandé de proposer en première intention un traitement chirurgical conservateur plutôt qu’un DIU au LNG 52 mg en raison d’un taux moindre d’effets secondaires.13
– Chez une femme adulte ayant des ménorragies idiopathiques et ne souhaitant pas conserver ses possibilités de procréation les données de la littérature ne permettent pas d’établir de recommandation préférentielle entre DIU LNG 52 mg et le traitement chirurgical non conservateur du fait de la bonne balance bénéfice risque de ces deux approches.
Ainsi les DIU au LNG 52 mg représentent le traitement de choix des ménorragies fonctionnelles avec une supériorité versus les autres traitements médicaux hormonaux et l’acide tranexamique :
– chez les femmes souhaitant conserver leurs possibilités procréatrices et/ou leur utérus, le DIU au LNG 52 mg est un traitement qui doit être préférée à la chirurgie
– chez les femmes ne souhaitant pas conserver leurs possibilités procréatrices et leur utérus, le DIU au LNG 52 mg est un traitement qui doit être mis en balance avec la chirurgie au cas par cas.
Christian Jamin est consultant pour le laboratoire Gédéon Richter France.
David Elia n’a pas de liens d’intérêt en relation avec cet article.
Christian Jamin, David Elia 75008 Paris
RÉFÉRENCES
1. Newton J, Barnard G, Collins W.A rapid method for measuring menstrual blood loss using automatic extraction. Contraception 1977 ;16 :269–82.
2. Haynes PJ, Hodgson H, Anderson AB, Turnbull AC. Measurement of menstrual blood loss in patients complaining of menorrhagia. Br J Obstet Gynaecol. 1977 ;84 : 763-8.
3. Munro MG, Critchley HO, Broder MS, Fraser IS FIGO Working Group on Menstrual Disorders. FIGO classification system (PALM-COEIN) for causes of abnormal uterine bleeding in nongravid women of reproductive age. Int J Gynaecol Obstet. 2011 Apr;113(1):3-13. doi: 10.1016/j.ijgo.2010.11.011. Epub 2011 Feb 22. PMID: 21345435.
4. Righini M, Gerber S, Hohlfeld P, Menorrhagia de Moerloose P., hypermenorrhea and disorders of hemostasis. J Gynecol Obstet Biol Reprod 1999 ;28 :413–8.
5. Froelich, S. et al. Does cyproterone acetate promote multiple meningiomas? Endocrine abstracts 16, P158 (2008)
6. Étude GIS EPI- PHARE, Acétate de cyprotérone et risque de méningiome, rapport final, juin 2019
7. CST-Macroprogestatifs et risque de méningiome, https://ansm.sante.fr/var/ansm_site/storage/original/application/ e5136e006bef14e2fc895887d590a0a1.pdf
8. Brun JL, Recommandations de pratique clinique sur les saignements utérins anormaux ou ménorragies, conference
de presse du CNGOF – janvier 2021
9. Moerloose, P., d., Gueddi, S., Boehlen, F., Ziegler, D., d. (2005). ‘Ménorragies et anomalies de l’hémostase : diagnostic et traitements’, Rev Med Suisse 2005 ; volume -9. no. 004, 279 – 282 doi:
10. Silva Clin Breast Canc 202 ;24 :7-23
11. Jareid Gynécol Oncol 2017
12. Luukkainen Semin Reprod Med 2001 ;19 :355-63
13. Bofill Rodriguez Cochrane Library 2020 Bergeron Hum Reprod update 2020
GENESIS – N° 206 – JUIN / JUILLET 2021








28 commentaires